
- 首页
- >
- GENESEED
- >
太阳成tyc33455cc客户丨单志新研究员团队设计circSP199a作为miRNA抑制剂,显著减轻心脏肥大和纤维化
广东省人民医院单志新研究员在Acta Pharmacol Sin期刊上发表研究论文:circSP199a, a circularized RNA sponge targeting miR-199a-5p and -3p, mitigates mouse cardiac hypertrophy and fibrosis。研究设计并合成了一种新型环状RNA分子海绵——circSP199a,以靶向抑制miR-199a-5p和-3p的功能,circSP199a在体外和体内模型中均有效缓解心脏肥大和纤维化,为心脏疾病治疗提供了潜在的策略。

心脏肥大和纤维化靶点发现
心力衰竭(HF)已成为全球公共卫生的沉重负担,其核心病理基础是进行性心脏重塑,表现为异常心肌肥大与纤维化。然而,迄今尚无获批药物可阻断这一过程。因此,靶向逆转心脏重塑的创新疗法,被视为破解心力衰竭困局的关键突破口。
团队前期研究表明,miR-199 a-5p和-3p在心脏重塑小鼠和人心肌中表达上调。miR-199a-5p和miR-199a-3p通过分别靶向抑制Ppargc1a和Sirt1、Rb1和Smad1的表达,协同加剧心脏肥大和纤维化。[1]
miR-199a-5p/-3p靶点验证
临床样本(心衰患者心肌)中,miR-199a-5p和-3p显著上调。在Ang II处理的新生小鼠心脏成纤维细胞(mCF)或PE处理的心室肌细胞(NRVC)中转染miR-199a-5p和-3p的inhibitor,可显著减轻心肌细胞肥大和心脏成纤维细胞的纤维化表型。
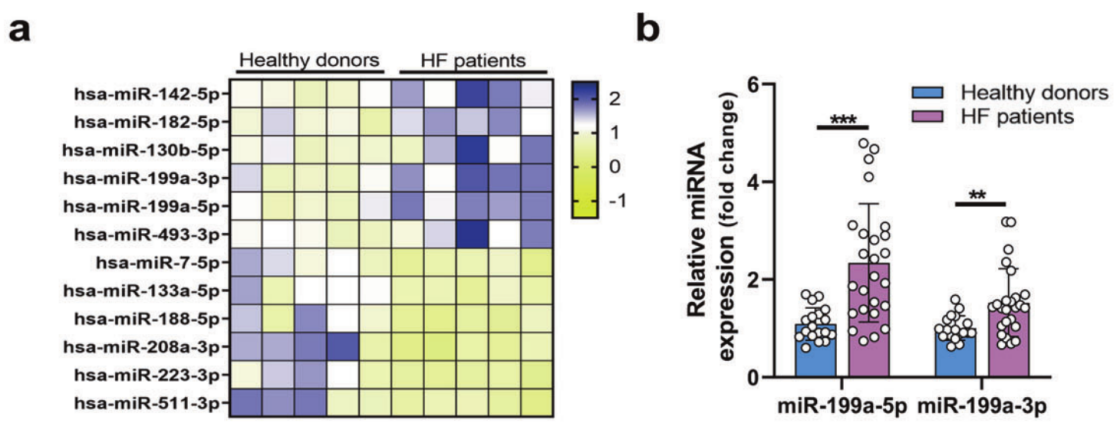
图1 miR-199a-5p和-3p在心衰患者心肌中表达上调。
候选药物circSP199a设计与合成
研究针对miR-199a-5p和-3p,设计了一种新型环状RNA分子海绵——circSP199a。circSP199a含有与miR-199a-5p和-3p种子序列反向互补的6个重复序列,长度为515 nt。
研究利用了太阳成集团tyc33455cc基于PIE的自研环化策略circPrecise®,体外精准、高效合成了circSP199a,并利用LiCl沉淀、太阳成tyc33455cc自研自产的RNase R处理等策略对产物进行纯化。circSP199a环化位点及在细胞中的稳定性得到了验证。
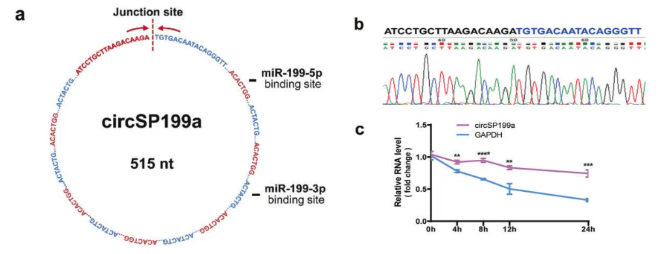
图2 a:环状RNA circSP199a的序列特征。b:通过Sanger测序测定circSP199a的环化位点。c:放线菌素D处理后HEK 293细胞中circS199 a和GAPDH mRNA的水平。
候选药物circSP199a设计与合成
脂质体转染circSP199a
研究利用太阳成集团tyc33455cc现货产品circ-eGFP,对脂质体(Lipofectamine 2000)转染circRNA条件进行了优化,最终实现了circSP199a向NRVC和mCF的有效转染。脂质体转染的circSP199a显著抑制了PE和Ang II诱导的miR-199a-5p和-3p的表达和功能,下调了心肌肥大和纤维化相关生物标志物的表达,并缓解了NRVC的细胞增大和mCF纤维化。
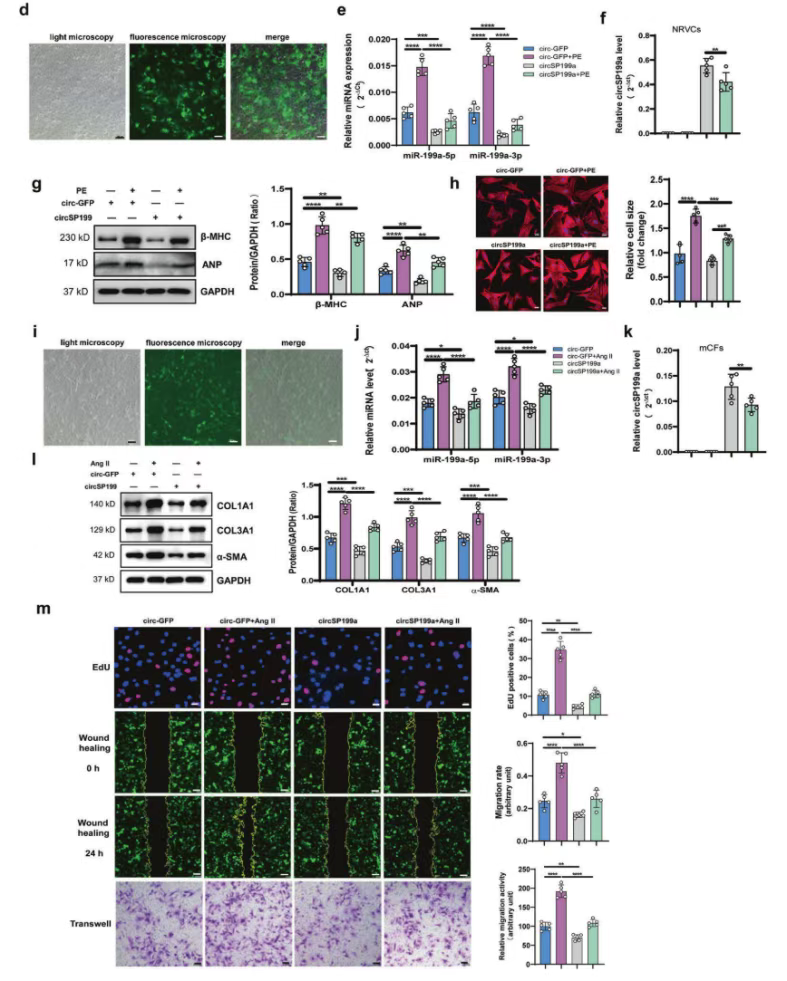
图4 体外合成的circSP199a抑制离体细胞模型的心脏肥大和纤维化。d-h:circSP199a对PE诱导的NRVC肥大的影响;i-m:circSP199a对Ang II诱导的MCF纤维化表型的影响。
腺病毒介导circSP199a表达
研究利用腺病毒作为circSP199a的载体,在NRVCs和mCFs中显著逆转miR-199a-5p和-3p诱导的心肌肥大和纤维化。RIP实验表明,circSP199a与miR-199a-5p和-3p的结合是由AGO 2特异性介导的。
腺病毒-circSP 199 a,在PE诱导的心肌肥大NRVC和Ang II诱导的纤维化mCF中,减轻NRVC肥大和mCF的纤维化表型;在氧-葡萄糖剥夺(OGD)处理的人心脏微血管EC(HVMEC)中,抑制HCMEC中的eNOS表达和活化,显著逆转了OGD处理对HCMEC增殖和迁移能力的抑制作用;在冷冻损伤诱导的纤维化的人类心脏类器官(CO)模型中,改善了冷冻损伤诱导的CO纤维化。
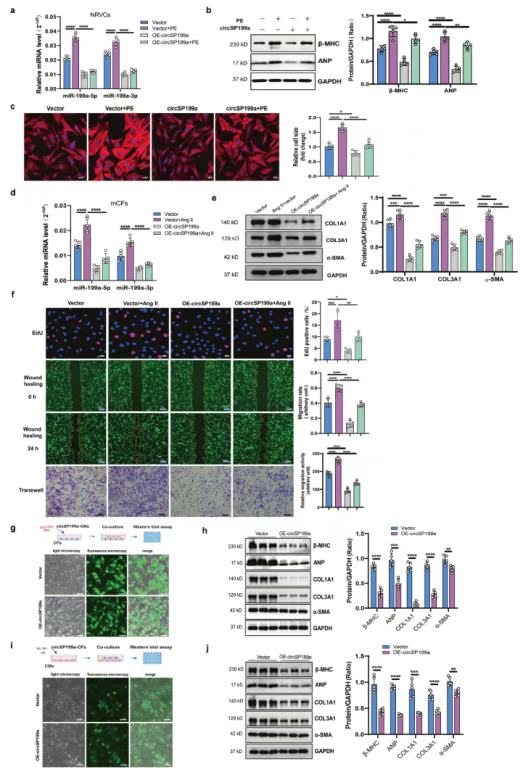
图5 腺病毒介导的circSP199a表达抑制苯肾上腺素诱导的心肌细胞肥大和Ang II诱导的心脏成纤维细胞纤维化表型。
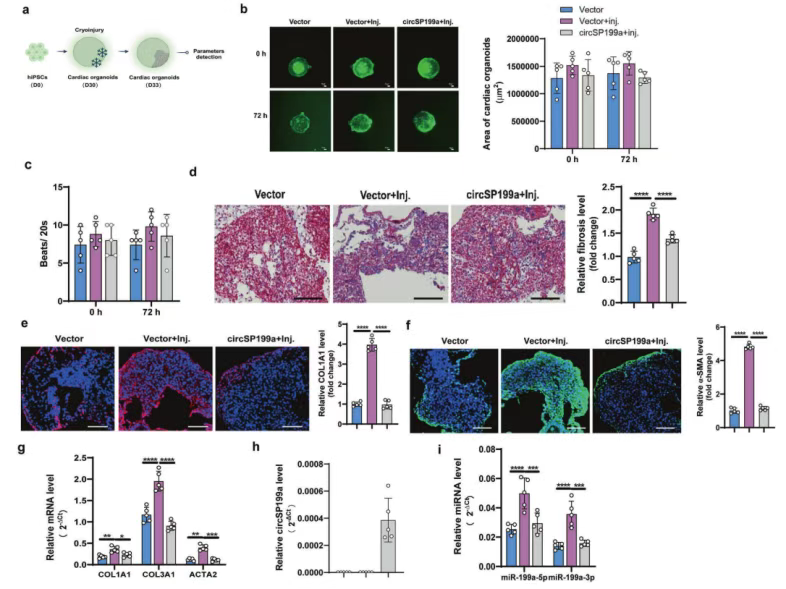
图6 腺病毒介导的circSP199a表达抑制了人类心脏类器官(CO)中冷冻损伤诱导的纤维化。
AAV9-circSP199a体内功效验证
研究还构建了腺相关病毒(AAV9)-circSP199a,TAC手术前三周将AAV9-circSP199a尾静脉注射到小鼠体内。AAV9-circSP199a通过抑制miR-199 a-5p和-3p的表达和功能,增强了靶基因PGC-1α、Rb1、Sirt1和Smad1的表达,减弱了TCA小鼠心肌肥大,改善了小鼠横主动脉收缩引起的心脏损伤和重塑。
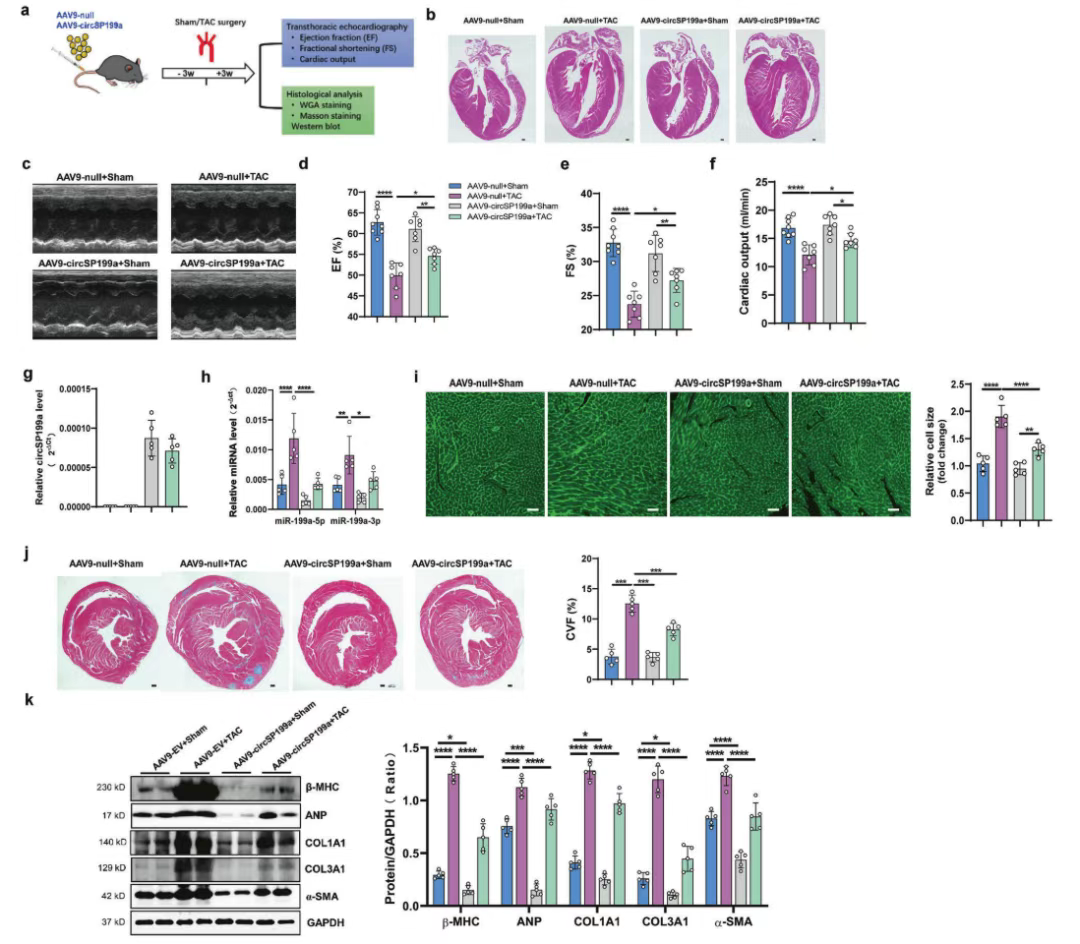
图7 AAV9介导的circSP199a表达抑制TAC小鼠的心脏肥大和纤维化。
总结
研究人工设计和合成了circSP199a,作为miR-199 a-5p和-3p的抑制剂。研究还在体外和体内验证了circSP199a可以显著改善心肌肥厚和纤维化的表型。circSP199a具有成为病理性心脏肥大和纤维化的疗法的潜力,也为基于circRNA分子海绵的疗法开发提供了新的见解。
虽然研究使用脂质体法(Lipofectamine 2000)将体外合成的circSP199a有效地转染到NRVC和mCF中,但该转染方法具有潜在毒性,且转染效率相对较低。研究下一步可能需要利用脂质纳米颗粒(LNP)递送circSP199a,进行更全面和深入的体外和体内研究,以探索circSP199a作为miRNA抑制剂,对心脏肥大和纤维化的治疗潜力。
原文链接
https://www.nature.com/articles/s41401-025-01620-9
参考文献
[1] Zeng N, et al. Diverging targets mediate the pathological roleof miR-199a-5p and miR-199a-3p by promoting cardiac hypertrophy and fibrosis. Mol Ther Nucleic Acids. 2021;26:1035-1050.

 购物车
购物车


 广州市黄埔区开源大道11号科技企业加速器A区6栋2楼
广州市黄埔区开源大道11号科技企业加速器A区6栋2楼


 geneseed@geneseed.com.cn
geneseed@geneseed.com.cn